PT认证!美康自研方法满分通过卫健委白血病BCR::ABL1室间质评
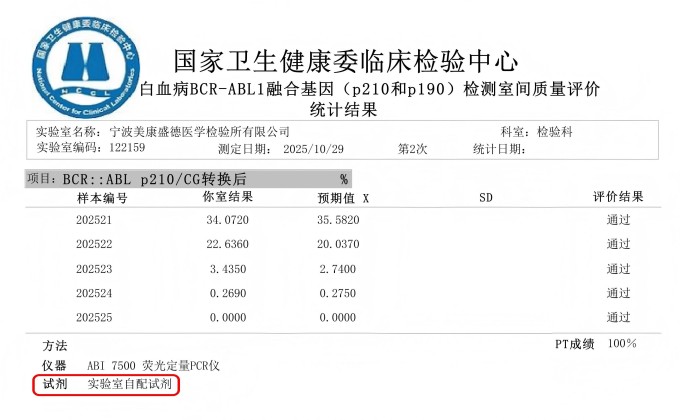
发布日期:2025/12/10 0:00:00近日,在国家卫生健康委临床检验中心(以下简称NCCL)公布的2025年全国白血病BCR::ABL1融合基因(p210)检测的实验室能力验证(Proficiency Test,PT)结果中,美康盛德医检凭借自主研发的RT-qPCR检测体系,以满分成绩通过验证。这标志着美康盛德医检的分子检测技术在血液病微小残留病(Measurable Residual Disease , MRD)监测的精确度与可靠性方面达到了国家权威认可的高标准。
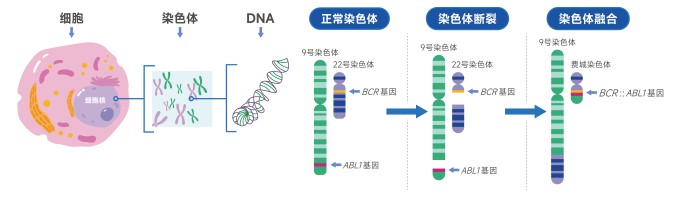
慢性髓性白血病(Chronic Myeloid Leukemia,CML)是一种起源于造血干细胞的恶性克隆性疾病,其标志性的费城染色体(Philadelphia chromosome,Ph)及BCR::ABL1融合基因不仅是诊断的金标准,也是关键的分子治疗靶点。监测BCR::ABL1(p210)转录本水平,对于CML患者的辅助诊断、疗效监测和预后判断至关重要[1]。长期、稳定地达到深度分子学反应(Deep Molecular Response,DMR)是患者实现无治疗缓解(Treatment-free Remission,TFR)的重要前提,而准确监测BCR::ABL1(p210)转录本水平,正是评估DMR、指导治疗决策、从而帮助患者获得高质量长期生存并减少不良反应的核心依据。因此,准确而稳定的分子学检测对CML的全程管理具有重大的临床意义[2-3]。
然而,由于内参基因的选择、试剂及仪器等多种因素影响,不同实验室对同份BCR::ABL1融合基因样本的检测结果往往存在差异,使得实验室间的结果难以直接比较。为实现国内实验室间的结果可比性,NCCL在本次PT活动中参考国际标准化组织的方式[4]:首先,组织180家参评实验室使用同一组参考物质进行检测;然后,将各实验室检测结果的均值与参考物质的给定真值进行线性回归分析,由此计算出各实验室的转化系数(Conversion Factor,CF);最终,通过该CF值可将实验室的质评样本原始检测结果转换为统一的BCR::ABL1IS值,从而实现国内不同实验室间检测结果的可比性。
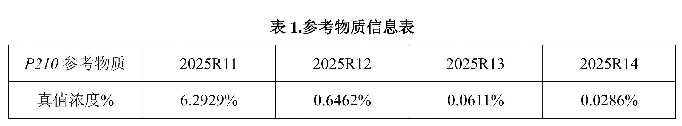
本次质评提供的参考物质(见表1),包含了融合比例6.2929%及其10倍、100倍和300倍梯度稀释的样本集,最低浓度达0.0286%,即相当于分子学反应MR 4.0水平(0.01%)。
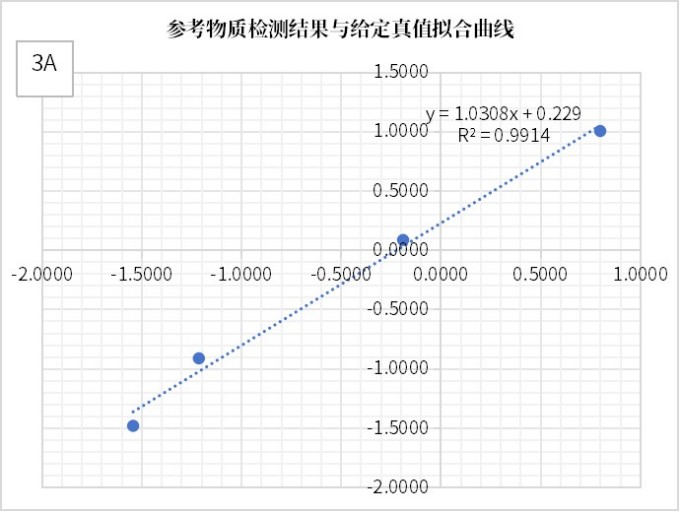
美康盛德医检实验室利用自主研发的检测体系进行分析,结果显示:检测值与真值的回归拟合度优异(R²=0.9914)(见图3-A),并由此获得转换系数CF=0.5902。进一步,将CF应用于质评样本的转换后结果,再与回报的预期靶值进行拟合分析,所得拟合度R²高达0.9967(见图3-B)。表明转换后的检测结果与预期靶值高度一致。
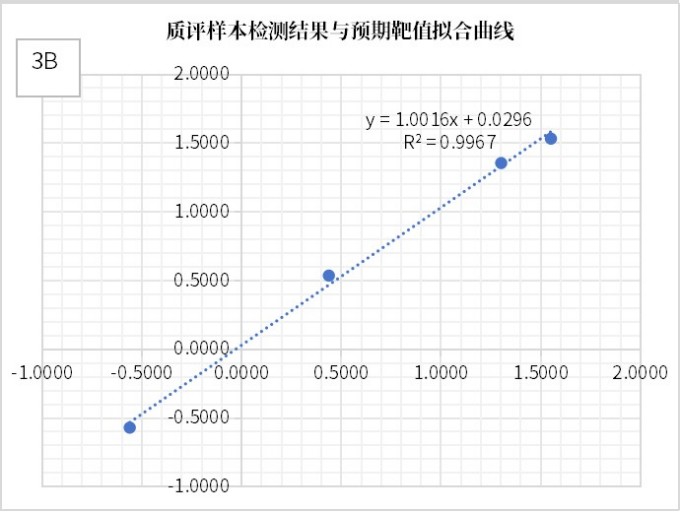
以上数据充分证实了美康自建检测体系具备优异的稳定性和准确性,能够稳定监测低至MR 4.0水平的BCR::ABL1转录本残留。该结果也为后续推进BCR::ABL1IS国际标准化奠定了坚实的技术基础。
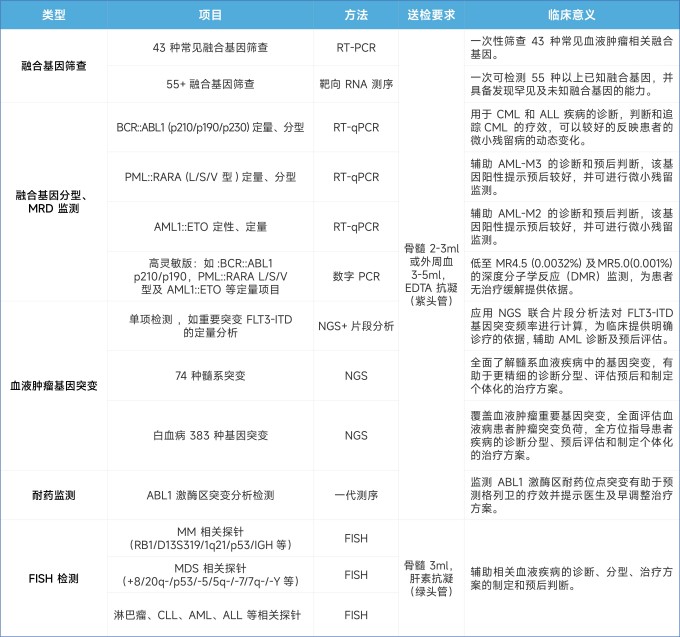
美康盛德医检依托RT-qPCR、数字PCR、NGS(二代测序)、纳米孔测序、FISH(荧光原位杂交)及一代测序等技术平台,构建了覆盖血液肿瘤全病程管理的分子检测体系,涵盖鉴别诊断、精准分型、预后评估、微小残留病(MRD)监测、风险分层与耐药监测等关键环节,为临床提供贯穿诊疗全程的精准决策依据。
参考文献:
[1]慢性髓性白血病诊疗指南(2022年版).
[2]Naranie S,et al. Early BCR-ABL1 kinetics are predictive of subsequent achievement of treatment-free remission in chronic myeloid leukemia[J].Blood,2021,137(9):1196-1207.
[3]Kockerols C, Valk PJM, Hogenbirk P,et al. Treatment‐Free Remission Outcomes in a BCR::ABL1 Digital PCR Selected Clinical Cohort of CML Patients[J].EurJ Haematol,2025,114(5):900-907.
[4]秦亚溱, 马道新, 王云贵, 等. 转换国际标准化的BCR-ABL(P210)转录本水平的转换系数多中心再确认研究[J].中华血液学杂志, 2015,36(10):814-817.







